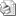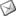Caso clínico de rehabilitación oral completa:
Paciente de 45 años
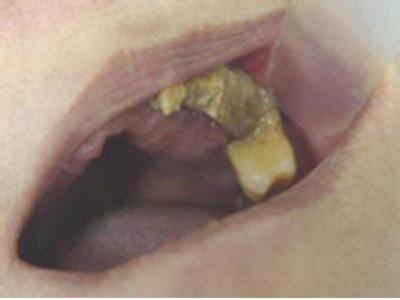
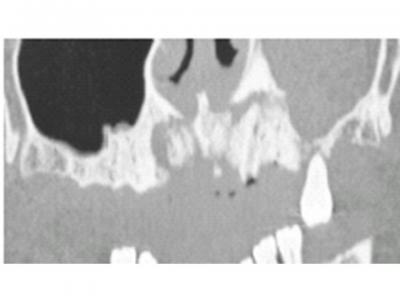
Presenta una situación periodontal avanzada con movilidad grado III en maxilar superior e inferior.
Se realizan exodoncias superiores e inferiores y colocamos unas prótesis completas.






Se colocaron prótesis provisionales superior e inferior durante dos meses.
A los dos meses se colocaron 6 implantes en maxilar superior sin cirugía guiada y 6 implantes inferiores con cirugía guiada y carga inmediata. El antagonista superior fue la prótesis completa que confeccionamos post- extracción.
Superior:

Inferior:
Carga inmediata inferior:
Protesis fija inferior con 6 implantes.

Incisión con bisturi circular atraves de la guia quirujica, y despegamiento del tejido.




Se realiza un fresado con la guía quirugica a baja velocidad sin utilizar la irrigación. La dificultad de irrigación de la fresa con la guía puede hacer que se recaliente el hueso con la consecuente necrosis del mismo.




Es importante que el diseño de la guía quirugica presente siempre tres agujas de fijación, para evitar movimientos.

La guía quirugica se realiza con un Tac y una férula radiológica (bario). Esta férula es una copia de la prótesis completa que se realizo al paciente cuando realizamos las exodoncias. Se escanea la férula radiologiaca y cuando se realiza el Tac y se superponen las informaciones recogiadas del paciente: los modelos (impresiones), la guía radiológica y el tac.
En este caso se presento una complicación en la colocación del implante del 43 por una perdida de la cortical vetibular. Se soluciono con una regeneración del defecto.


Retiramos la guía y realizamos la regeneración.

El resto de los implantes ya estaban colocados.






Preformamos la membrana para adaqptarla al defecto. En el tac ya teniamos información de la perdida de la cortical vestibular. (no nos pillo de sorpresa)


Cerramos y suturamos. La orientación de este implante se modifico un milimetro de lo planificado en el ordenador. Esto supuso preformar la prótesis de carga inmediata a este nivel.

Se coloca la prótesis con carga inmediata inferior.


Se realiza el ajuste oclusal.


Esperamos un total de 4 meses para la colocación de la prótesis definitiva.




El diastema inferior fue a petición de la paciente para que pareciera mas natural.

 ¿Cuanto tiempo le quedan a los implantes dentales?
¿Cuanto tiempo le quedan a los implantes dentales?